【高尚病例】肺泡蛋白沉积症
病史摘要
某先生,51岁,咳嗽、咳痰(白色)1年余,2019年09月外院CT诊断:右下叶片状增密影。
穿刺病理:少许肺组织、纤维组织及横纹肌组织、局灶间质组织略增生。
纤维支气管镜肺泡灌洗液未发现抗酸菌,灌洗液病理:肺组织、肺泡腔见较多泡沫样组织细胞聚集。
该患者曾行实验性抗结核治疗3月,复查病灶无明显变化,中药治疗至今,目前走路气喘、胸闷。既往无殊,职业为办公室职员,无粉尘接触史。
PET/CT影像图
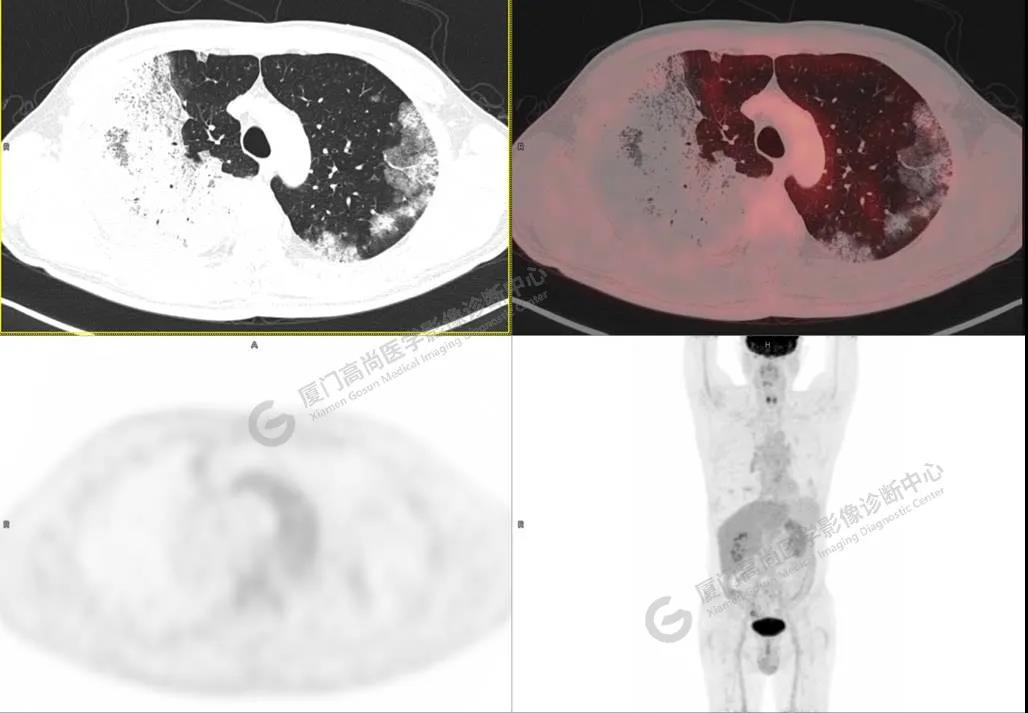
图1
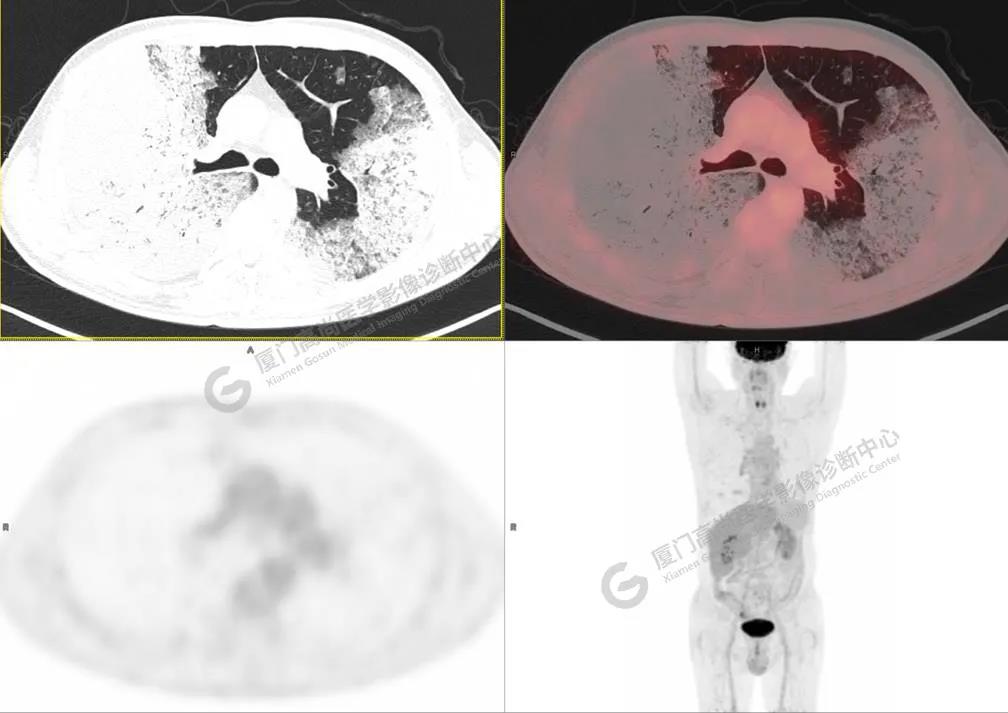
图2
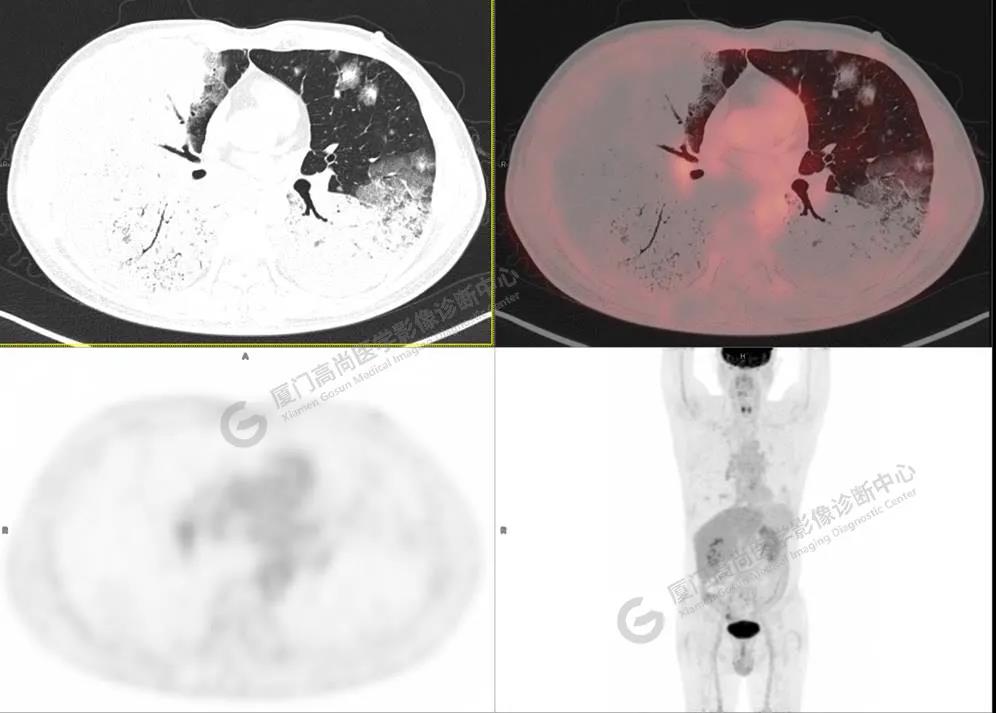
图3
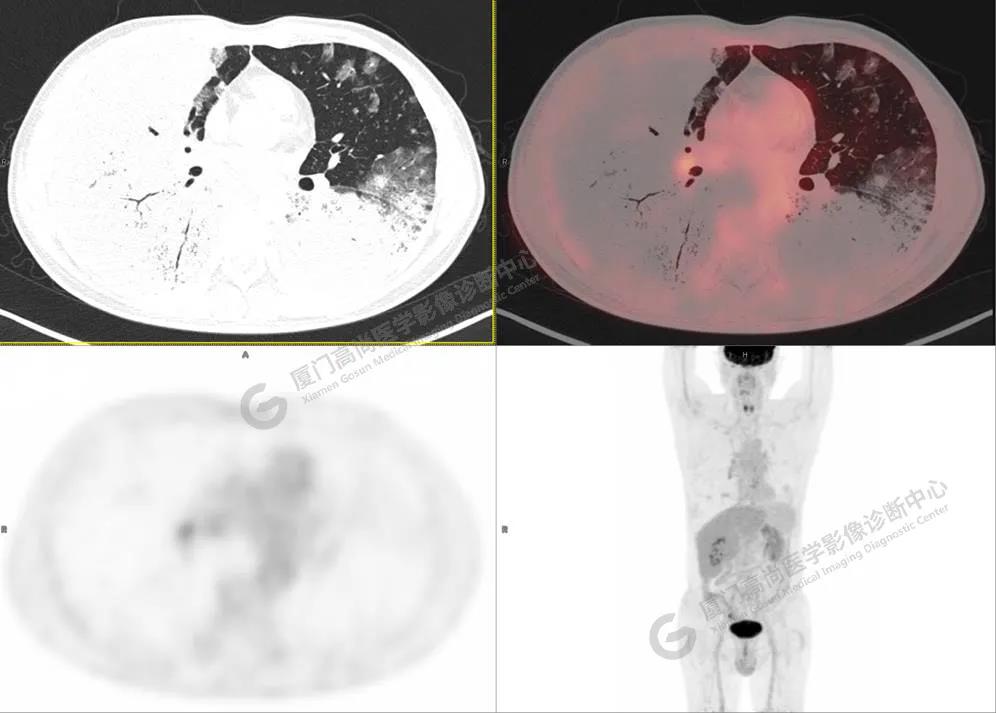
图4
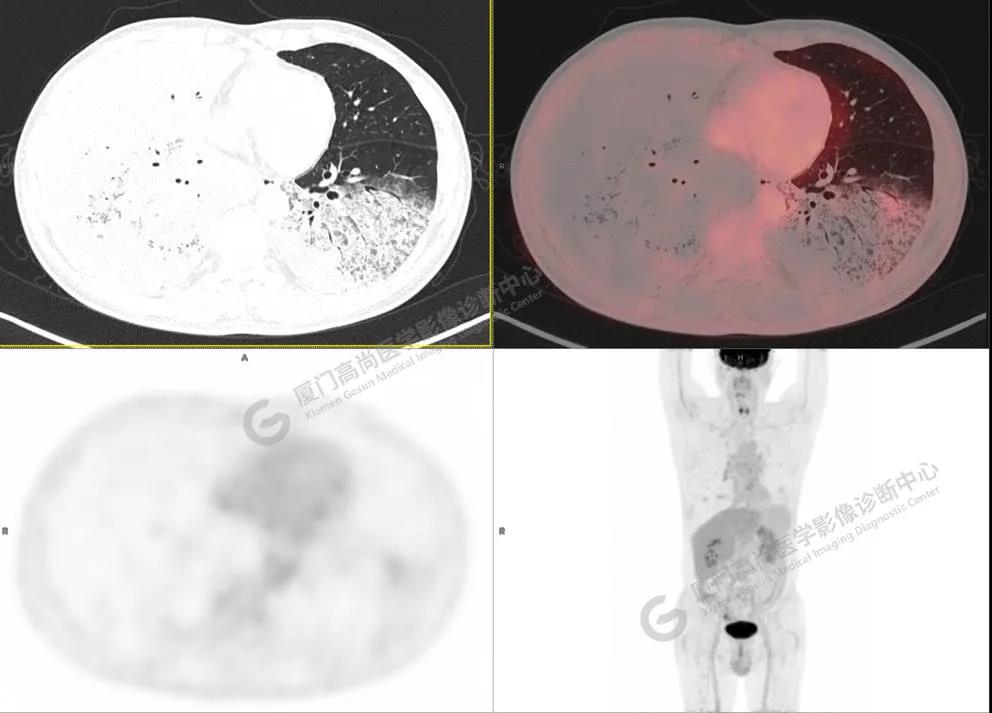
图5
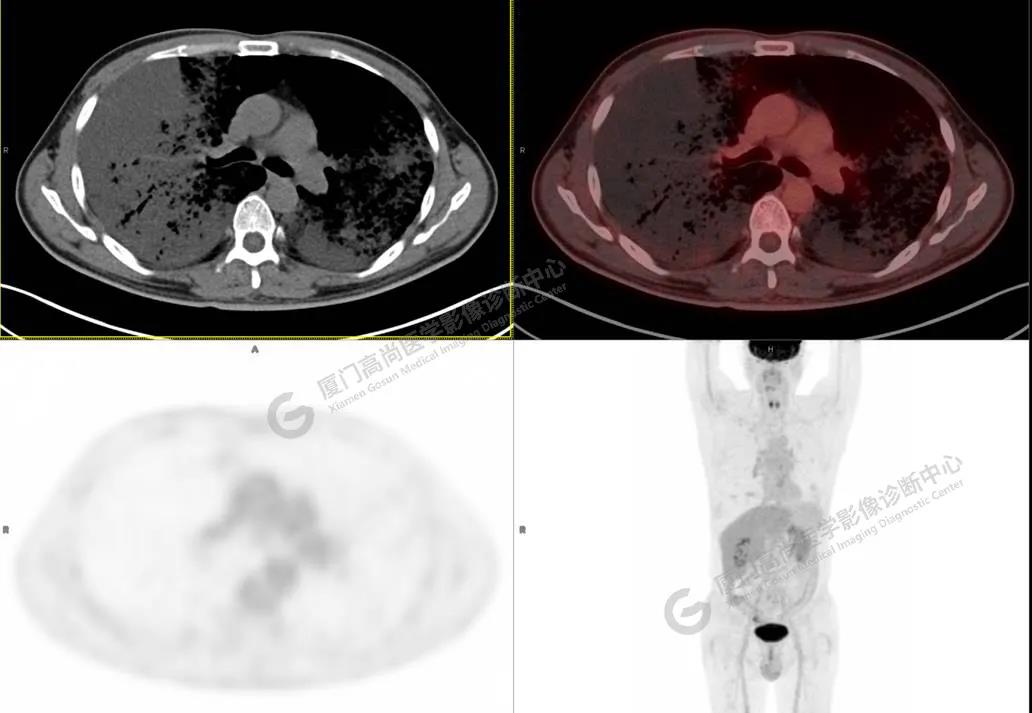
图6
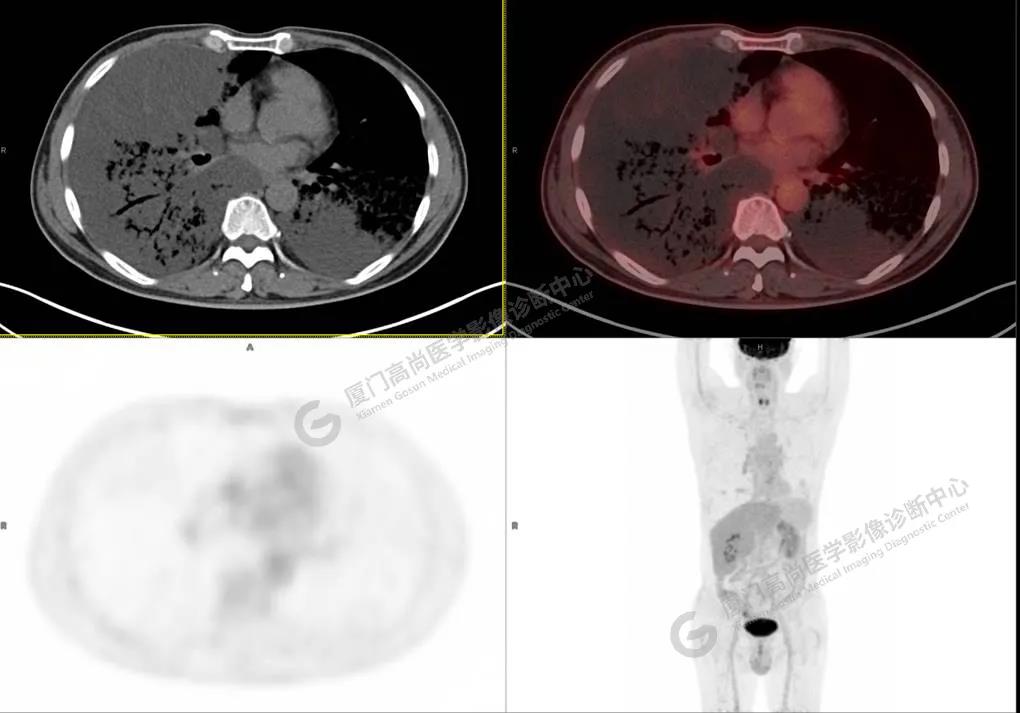
图7
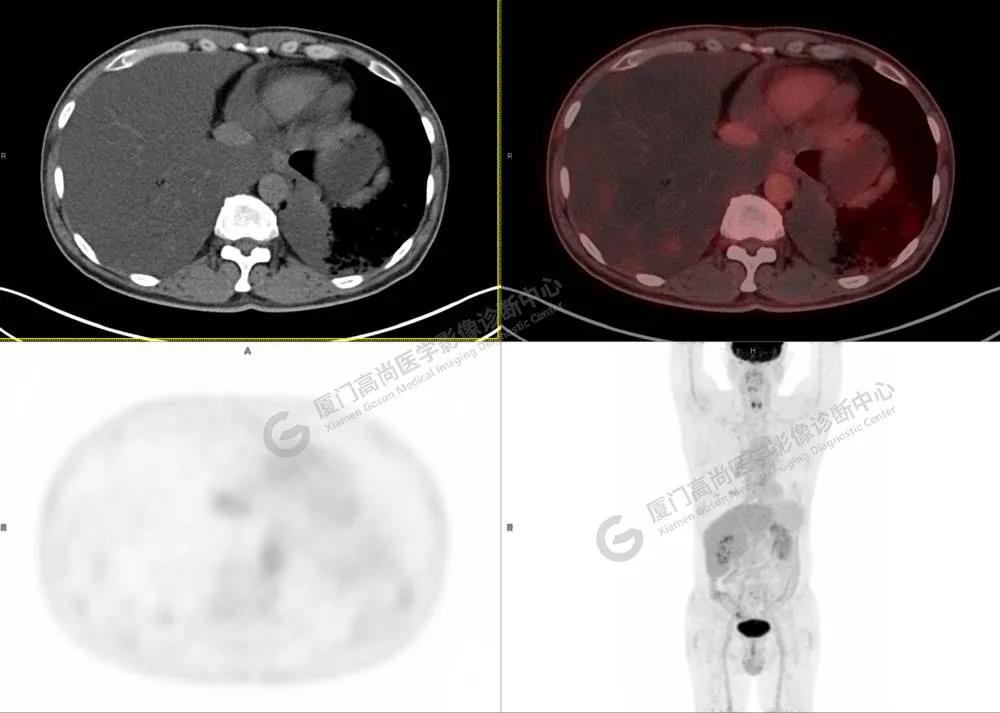
图8
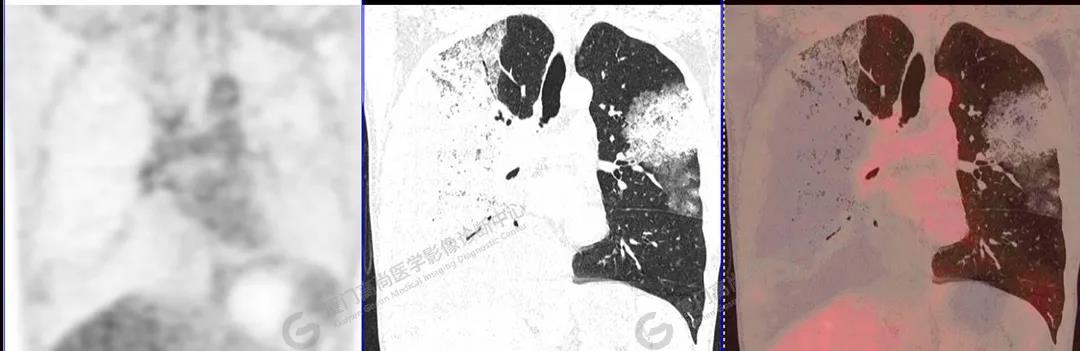
图9
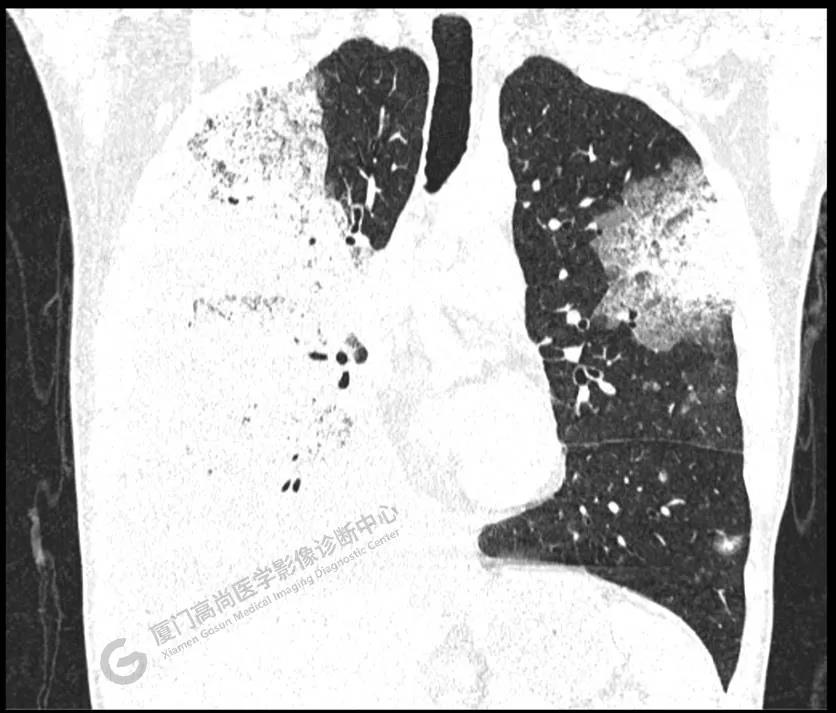
图10
PET/CT检查
PET/CT所见:双肺大片实变影及磨玻璃影,部分呈地图样改变,累及右肺尖,部分放射性摄取轻微增高,SUVmax 1.77,其内见多发支气管充气征象。
影像诊断: 双肺大片实变影及磨玻璃影,大部分代谢不高,局部代谢轻微增高,考虑肺泡蛋白沉积症,建议病理学检查或肺泡灌洗物检查。
肺泡蛋白沉积症概述
概述及发病机制:肺泡蛋白沉积症(PAP),又称肺泡磷脂沉着症,是一种亚急性、进行性呼吸功能不良疾病及罕见的弥漫性肺部疾病,其特征为PAS染色阳性的磷脂蛋白在肺泡腔内大量聚集,可分为3种类型:原发性,继发性和先天性。
原发性PAP是由粒细胞巨噬细胞集落刺激因子(GM-CSF)自身抗体(即自身免疫性PAP,90%以上)或涉及GM-CSF受体遗传突变(即遗传性PAP,约占30%)引起的GM-CSF失活造成的。
继发性PAP主要由血液系统疾病、感染或吸入有毒物质引起,使肺泡巨噬细胞数量减少或功能散失,约占4%。
先天性PAP示由正常表面活性剂生产所需的基因突变引起的,约占1.5%。
病理:主要是肺泡及细支气管内有嗜酸PAS强阳性物质充填,是II型肺泡细胞产生的表面活性物质磷脂与肺泡内液体中的其他蛋白质和免疫球蛋白的结合物,其成分为糖蛋白和磷脂。肺泡间隔及周围结构完整。支气管肺泡灌洗液呈米汤样或豆腐渣样白色浑浊,静置后有沉淀,是其典型特征。
影像学表现:HRCT上双肺斑片影,以肺门为中心呈蝶翼状对称分布;病变可随机分布在中央区、周围区或全肺叶,病灶与正常分组织分界清楚,呈典型“地图样”改变;有支气管充气征,但表现为充气支气管细小且数量及分布稀少;“碎石路”征由弥漫性磨玻璃影及内部网格样小叶间隔增厚组成(铺路石样表现)。无空洞、蜂窝状改变、淋巴结肿大、胸腔积液及明显实变等。肺内病灶累及范围、磨玻璃密度高低与PAP患者的病情严重程度相关,严重者病灶累及全肺,同时出现肺内大片实变,并见充气支气管征象。PAP影像学表现程度与临床症状、体征严重程度不成比例,表现为影像改变重,临床症状轻。
鉴别诊断
卡氏肺孢子菌肺炎(PCP):病变进展迅速,较快累及全肺;多见细小空洞形成,多发生在血液病晚期、极度衰竭期、免疫缺陷患者;机遇性感染患者。
特发性含铁血黄素沉着症:多见于儿童,临床表现反复咯血、气促、贫血;影像变化较快,2-3天可明显吸收;患者痰中或胃液内可见含铁血黄素细胞;普鲁士蓝反应阳性。
肺水肿:边缘模糊斑片影,肺门周围“蝶翼”征,多有明显心脏增大;临床症状明显。
弥漫性肺炎:明显发热病史;短期抗炎治疗有效果,多单侧发病,以肺叶或肺段分布为主。
作者简介

郭秀梅
核医学科 执业医师
毕业于湖南中医药大学医学影像专业,曾于广州医科大学附属第一医院参加住院医师规范化培训,熟悉常见病的影像诊断,包括PET/CT,DR,CT,MRI。对疑难疾病有一定的诊断思路。熟悉CT三维后处理,包括冠脉后处理,各种血管重建,骨重建等。

